超強酸性炭素酸の合成と利用
「巨大プールに水を満たし,一滴の濃硫酸を加えました。さて,プールの水は強い酸性を示すでしょうか?」
この問いは,媒体の酸性度と分子の酸性度の区別を際立たせます。媒体の酸性度(酸強度)、つまり酸分子の水溶液がそこに溶けた溶質をプロトン化する能力は,通常,pH で表します。他方,酸分子が別の分子にプロトンを渡す能力である分子の酸性度は,pKa 値などによって定義されます。
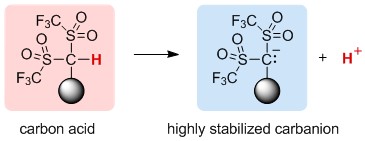
有機化学の教科書は,炭素上に解離性水素をもつ「炭素酸」に関する説明に多くのページを割いています。1,3-ジカルボニル化合物などの活性メチレン化合物が,有機合成上,極めて重要な出発原料となっているためです。ただし,こうした活性メチレン化合物が酸として機能するといっても,その pKa 値はフェノールと同程度で,硫酸分子のような無機酸にくらべれば圧倒的に酸性度は弱いというのが一般的な理解です。「C-H」構造をもつ化合物(炭素酸)の酸性度は,フェノールと同程度か,それに少し負けるくらいというレベルなのです。
ところが,1960年代中頃,ビス(トリフリル)メタン(Tf2CH2, Tf = CF3SO2)が合成され,それが硫酸に匹敵する強酸性分子であることが報告されました。しかし,あまりに珍しい存在であったことから,今世紀に至るまで長らく注目されることはありませんでした。私たちは,合成法がほとんど知られていない超強酸性炭素酸Tf2CHRの合成手法を開発し,得られた酸性度の評価と化学構造の解明,酸触媒としての利用を検討してきました。[1]
私たちは,まず,1,1,3,3-テトラキス(トリフリル)プロパン Tf2CHCH2CHTf2 1 に着目し,これが気相では硫酸分子をはるかに超える超強酸分子であることを見いだしました。また同時に,トリフルオロメタンスルホン酸 TfOH やビス(トリフリル)イミド Tf2NH といった既知の強酸よりも圧倒的に高い触媒性能を示すことも報告しました。[2-4]
次いで,独自に開発した合成法を駆使することで,スルホン β 位に分岐差をもつ炭素酸 2 やベンゼン-1,3,5-トリオール構造に三つのTf2CH基を配した三価炭素酸 3 を開発しました。[5] 三価炭素酸 3 は,気相,溶液中のいずれにおいても硫酸分子よりも強い酸性度を呈する超強酸分子として注目に値するのみならず,既存の酸触媒では引き起こせないような難易度の高い分子変換がうまく進行させる高活性触媒として機能します。[6,7] 最近では,炭素酸構造を導入した生物活性分子の合成にも成功しています。[8]

私たちの研究成果は多くの研究者の関心を集め,現在では世界各国で「炭素酸触媒」の開発が進められるようになっています。
参考文献
- 矢内 光,田口武夫,有機合成化学協会誌, 2014, 72, 158.
- Takahashi, A.; Yanai, H.; Taguchi, T. Chem. Commun. 2008, 2385.
- Yanai, H.; Takahashi, A.; Taguchi, T. Chem. Commun. 2010, 46, 8728.
- Yanai, H.; Fujita, M.; Taguchi, T. Chem. Commun. 2011, 47, 7245.
- Yanai, H.; Ogura, H.; Fukaya, H.; Kotani, A.; Kusu, F.; Taguchi, T. Chem. Eur. J.2011, 17, 11747.
- Yanai, H.; Taguchi, T. Chem. Commun. 2012, 48, 8967.
- Yanai, H.; Kobayashi, O.; Takada, K.; Isono, T.; Satoh, T.; Matsumoto, T. Chem. Commun. 2016, 52, 3280.
- Almendros, P.; Yanai, H.; Hoshikawa, S.; Aragoncillo, C.; Lázaro-Milla, C.; Toledano-Pinedo, M.; Matsumoto, T.; Alcaide, B. Org. Chem. Front. 2018, 53163.
